

光学成像(Optical Imaging),由于其具有非侵入性、实时、快速反馈和高灵敏度的优点,在生物医学分析中起着至关重要的作用。然而,由于复杂生物器官和组织中的内源性荧光团(黑色素,弹性蛋白,胶原蛋白,角蛋白,卟啉和黄素等)在外部辐射激发下会产生自发荧光,这使得活体荧光成像背景信号升高,从而限制了成像的信噪比(Signal-to-Noise Ratio, SNR)。因此,生物发光成像(Bioluminescence Imaging)由于其优异的生物相容性以及不需要外部激发光的特点受到了极大关注。迄今为止,生物发光成像已被广泛用于跟踪细胞,监测基因表达,检测生物活性小分子,肿瘤成像等领域。然而,常规的基于荧光素酶(Luciferase)的生物发光探针发射波长大多位于可见光范围(VIS,400 nm-700nm),这使得在将其应用于生物成像时会受到生物组织的吸收和散射干扰,难以获理想的成像结果。尽管通过生物发光共振能量转移(Bioluminescence resonance energy transfer (BRET))策略,生物发光探针的发射波长能够被拓展到具有较低组织吸收的近红外第一窗口(NIR-I,700 nm-900 nm)。但散射效应仍然是一个障碍。近年来的研究表明在近红外第二窗口(NIR-II,1000-1700 nm)生物组织具有较小的吸收和散射。因此开发发射波长位于近红外第二窗口的生物发光探针将有利于提高生物活体成像穿透深度和信噪比,具有重要的应用价值。
为了解决这一挑战,张凡教授研究团队(http://nanobiolab.fudan.edu.cn/)设计合成了一种新型七甲川菁染料FD-1029。该染料的发射波长位于近红外第二窗口(1029 nm),且分子间具有较大的空间位阻,在较高浓度下不易发生聚集,能够拥有较大的摩尔消光系数。在这基础上,通过一步生物发光共振能量转移(BRET)和两步荧光共振能量转移(FRET)的设计策略实现了发射位于近红外第二窗口的新型生物发光探针(NIR-II-Bioluminescence Probes, NIR-II-BPs)。
该探针具有良好的生物相容性,成功应用于小鼠的血管和淋巴管的高信噪比成像。同时,由于这种能量传递策略的可调性,这类探针也能应用于多个目标物的多通道活体成像标记。作者进一步利用该探针对三磷酸腺苷(ATP)的特异性响应,结合肿瘤组织旺盛的新陈代谢所产生的ATP,成功实现了对淋巴结转移瘤的高信噪比成像追踪。由于无需外加激发光源,近红外第二窗口生物发光成像能够获得高达83.4的肿瘤/正常组织信号比(Tumor to Normal tissue Ratio),这一数值是同一体系中荧光成像的33倍。
这一成果近期发表在Nature Communications上,张凡教授和凡勇青年研究员为该论文共同通讯作者,博士生陆凌飞为论文第一作者。该工作得到了复旦大学化学系、复旦大学先进材料实验室、聚合物分子工程国家重点实验室、上海市分子催化与功能材料重点实验室、国家重大研究计划项目、国家自然科学基金杰出青年基金、上海市科学技术委员会重点基础研究项目的大力支持。
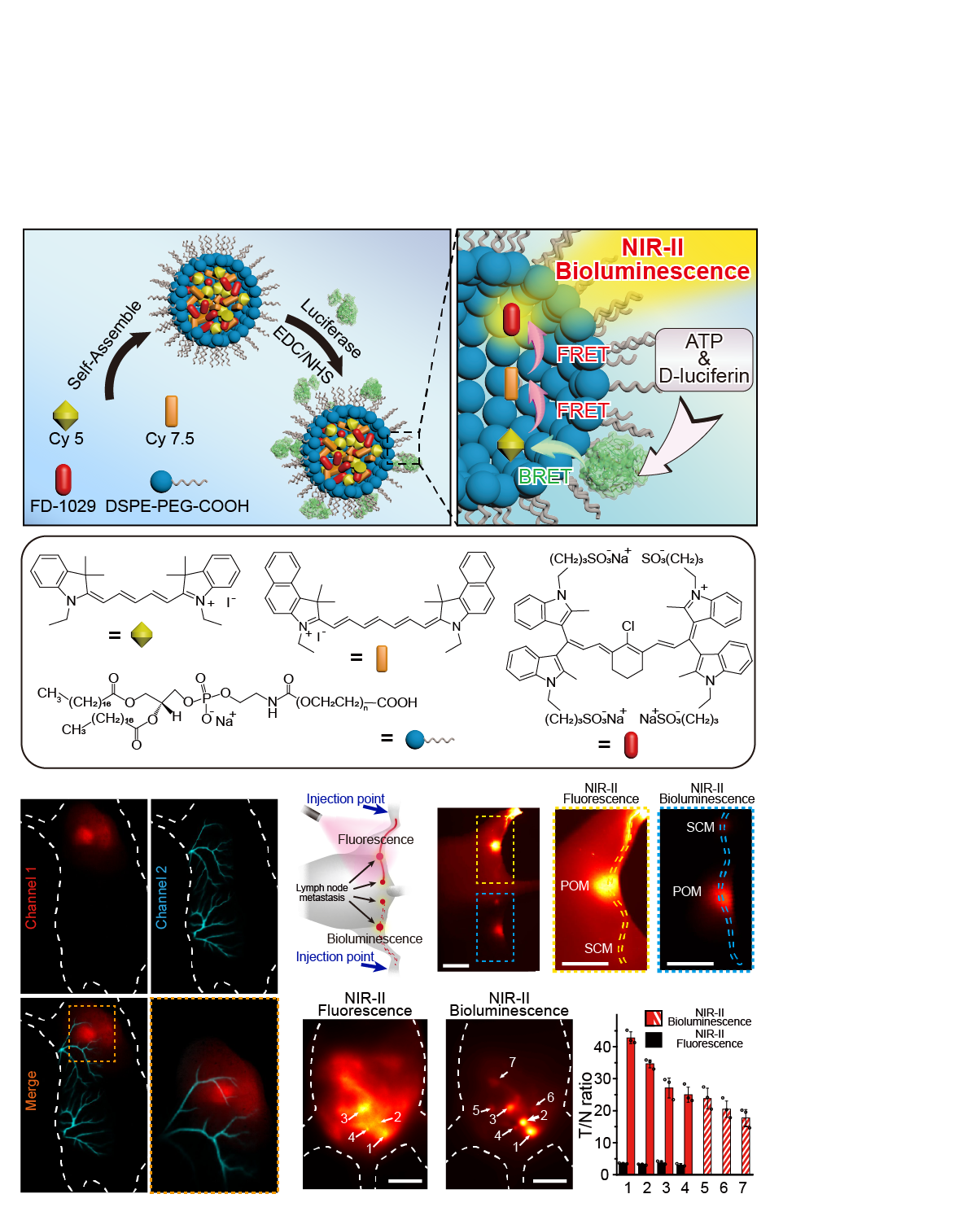
图1 近红外第二窗口发光的生物发光探针的制备原理及其在活体成像中的应用





