

过渡金属催化的烯丙基取代反应(Tsuji-Trost反应)已成为构建碳碳和碳杂原子键的有力工具。通过选择合适的配体,利用过渡金属催化剂,包括Pd、Ir、Rh、Ru、Co、Cu、Mo、W和Ni,可实现关键π-烯丙基金属中间体亲核取代过程中的区域和立体选择性控制,从而实现区域或立体单一的有机化合物合成。另一方面,结合化学键的迁移和偶联过程的迁移偶联反应显示出独特的区域选择性控制,例如多次1,2-氢迁移可以使碳-金属键通过烯烃-金属中间体(olefin-[M]-Int)进行链“行走”,从而实现偶联反应的远程选择性。相比之下,烯丙基金属中间体的整体迁移过程仍未被探索,过程中π烯丙基金属物种通过多个1,4-氢迁移在碳链上“行走”。
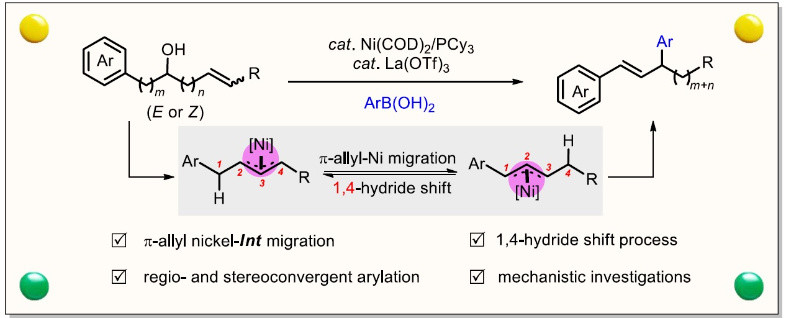
近日,我系朱灿课题组以非活化1,n-烯醇为模板底物,首次观察到烯丙基金属中间体的整体迁移过程,以此发展了镍-Lewis酸协同催化区域与立体选择性的芳基化反应。氘标记实验证实反应发生了特定的1,4-氢迁移;DFT理论计算研究表明π-烯丙基金属的迁移是由连续的β-H消除和迁移插入组成。在一个迁移周期中,以双烯-金属配合物(diene-[M]-Int)为关键中间体,发生连续的β-H消除和迁移插入。该方法具有广泛的芳基硼酸和1,n-烯醇底物范围,为构建具有独特选择性的C(sp2)-C(sp3)键提供了一种简便的合成策略。
这一研究成果以“Migratory allylic arylation of 1,n-enols enabled by nickel catalysis”为题发表在Nature Communications。复旦大学化学系博士研究生赵丹和博士后许冰为论文的共同第一作者,朱灿青年研究员为论文通讯作者。该工作得到了国家自然科学基金和复旦大学启动基金的资助。
全文链接:https://www.nature.com/articles/s41467-023-38865-z





